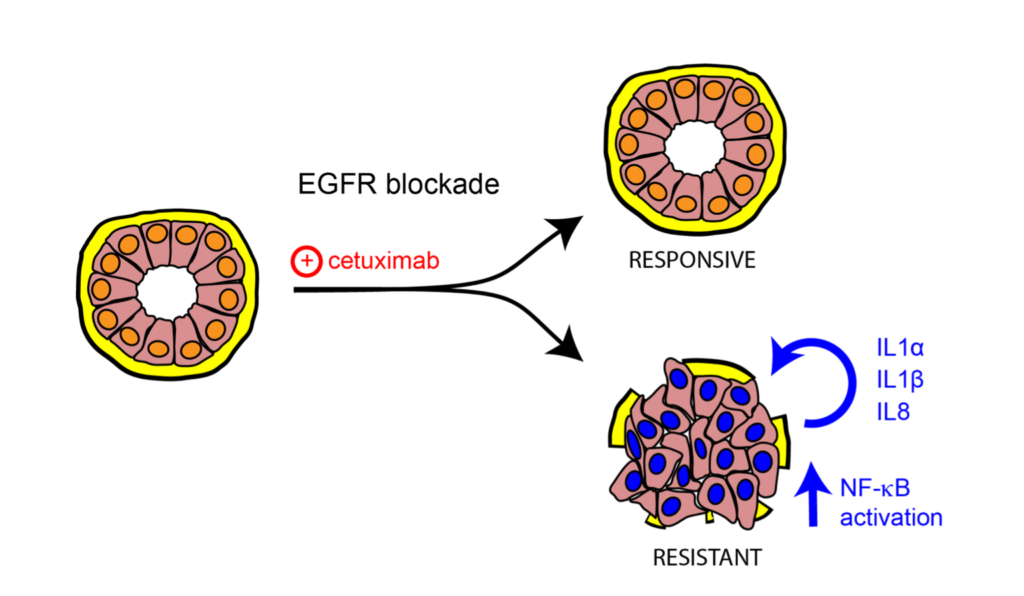
Epidermal Growth Factor Receptor (EGFR) activates a robust signalling network to which colon cancer tumours often become addicted. Cetuximab, one of the monoclonal antibodies targeting this pathway, is employed to treat patients with colorectal cancer. However, many patients are intrinsically refractory to this treatment, and those who respond develop secondary resistance along time. Mechanisms of cancer cell resistance include either acquisition of new mutations or non genomic activation of alternative signalling routes. In this study, we employed a colon cancer model to assess potential mechanisms driving resistance to cetuximab. Resistant cells displayed increased ability to grow in suspension as colonspheres and this phenotype was associated with poorly organized structures. Factors secreted from resistant cells were causally involved in sustaining resistance, indeed administration to parental cells of conditioned medium collected from resistant cells was sufficient to reduce cetuximab efficacy. Among secreted factors, we report herein that a signature of inflammatory cytokines, including IL1A, IL1B and IL8, which are produced following EGFR pathway activation, was associated with the acquisition of an unresponsive phenotype to cetuximab in vitro. This signature correlated with lack of response to EGFR targeting also in patient-derived tumour xenografts. Collectively, these results highlight the contribution of inflammatory cytokines to reduced sensitivity to EGFR blockade and suggest that inhibition of this panel of cytokines in combination with cetuximab might yield an effective treatment strategy for CRC patients refractory to anti-EGFR targeting.
Vai all’articolo originale (in inglese) : Gelfo V, Rodia MT, Pucci M, Dall’Ora M, Santi S, Solmi R, Roth L, Lindzen M, Bonafè M, Bertotti A, Caramelli E, Lollini PL, Trusolino L, Yarden Y, D’Uva G* and Lauriola M. A module of inflammatory cytokines defines resistance of colorectal cancer to EGFR inhibitors. Oncotarget 2016 (*co-last author)

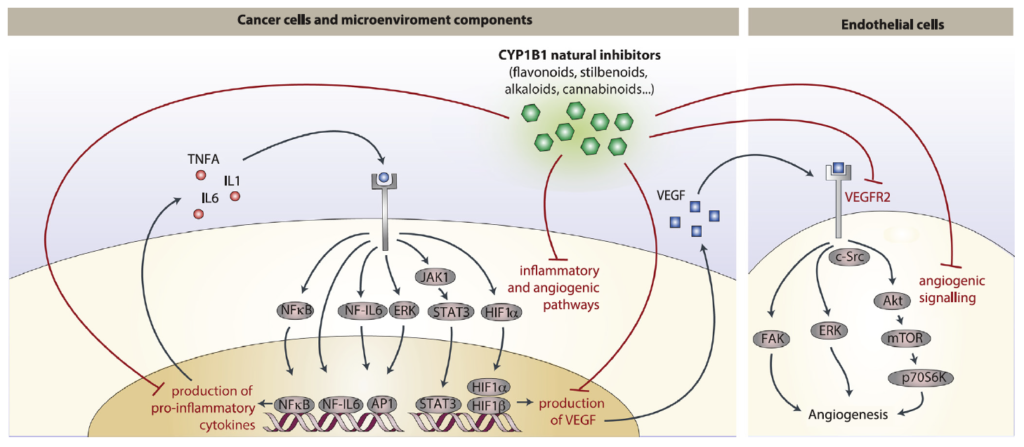 Sommario: La chemioprevenzione del cancro è una strategia basata sull’uso di agenti sintetici, naturali o biologici per prevenire o ritardare lo sviluppo o la progressione dei tumori maligni. Abbiamo notato che molte sostanze fitochimiche (ovvero naturalmente presente in alcune piante) dotate di effetti anti-infiammatori e anti-angiogenici e recentemente proposte come strategie di chemioprevenzione, sono inibitori della famiglia 1B1 del citocromo P450 (CYP1B1), un enzima sovraespresso in un’ampia varietà di tumori e associato ad angiogenesi (ovvero lo sviluppo di nuovi vasi che possono aiutare a disseminare le cellule tumorali). A loro volta, varie citochine infiammatorie possono aumentare l’espressione di CYP1B1, suggerendo un ruolo chiave di CYP1B1 in un ciclo positivo di angiogenesi infiammatoria. Altre attività pro-tumorigeniche ben note di CYP1B1 si basano sulla bioattivazione di xenobiotici e ormoni steroidei nei loro derivati cancerogeni. Contrariamente ad osservazioni iniziali in vitro, studi in vivo hanno dimostrato un ruolo protettivo contro il cancro per gli altri membri della famiglia CYP1 (CYP1A1 e CYP1A2), suggerendo che la specificità degli inibitori della famiglia CYP1 deve essere attentamente considerata per lo sviluppo di potenziali strategie di chemioprevenzione. Studi recenti hanno anche proposto un ruolo di CYP1B1 in diversi tipi di cellule presenti nel microambiente tumorale, compresi fibroblasti, cellule endoteliali e globuli del sistema immunitario. Nel complesso, la nostro studio della letteratura attuale suggerisce un ciclo positivo tra citochine infiammatorie e CYP1B1, che a sua volta può giocare un ruolo chiave nell’angiogenesi del cancro, agendo sia su cellule tumorali che sul microambiente. Strategie che mirano all’inibizione specifica di CYP1B1 in più tipi di cellule possono tradursi in un approccio clinico alla chemioprevenzione e angioprevenzione.
Sommario: La chemioprevenzione del cancro è una strategia basata sull’uso di agenti sintetici, naturali o biologici per prevenire o ritardare lo sviluppo o la progressione dei tumori maligni. Abbiamo notato che molte sostanze fitochimiche (ovvero naturalmente presente in alcune piante) dotate di effetti anti-infiammatori e anti-angiogenici e recentemente proposte come strategie di chemioprevenzione, sono inibitori della famiglia 1B1 del citocromo P450 (CYP1B1), un enzima sovraespresso in un’ampia varietà di tumori e associato ad angiogenesi (ovvero lo sviluppo di nuovi vasi che possono aiutare a disseminare le cellule tumorali). A loro volta, varie citochine infiammatorie possono aumentare l’espressione di CYP1B1, suggerendo un ruolo chiave di CYP1B1 in un ciclo positivo di angiogenesi infiammatoria. Altre attività pro-tumorigeniche ben note di CYP1B1 si basano sulla bioattivazione di xenobiotici e ormoni steroidei nei loro derivati cancerogeni. Contrariamente ad osservazioni iniziali in vitro, studi in vivo hanno dimostrato un ruolo protettivo contro il cancro per gli altri membri della famiglia CYP1 (CYP1A1 e CYP1A2), suggerendo che la specificità degli inibitori della famiglia CYP1 deve essere attentamente considerata per lo sviluppo di potenziali strategie di chemioprevenzione. Studi recenti hanno anche proposto un ruolo di CYP1B1 in diversi tipi di cellule presenti nel microambiente tumorale, compresi fibroblasti, cellule endoteliali e globuli del sistema immunitario. Nel complesso, la nostro studio della letteratura attuale suggerisce un ciclo positivo tra citochine infiammatorie e CYP1B1, che a sua volta può giocare un ruolo chiave nell’angiogenesi del cancro, agendo sia su cellule tumorali che sul microambiente. Strategie che mirano all’inibizione specifica di CYP1B1 in più tipi di cellule possono tradursi in un approccio clinico alla chemioprevenzione e angioprevenzione.